藥事法除了規範藥物、藥商及藥局之管理外,近年又增訂了第四章之一,有關於西藥之專利連結的規定,是醫藥領域中相當重要的法規。然而,市面上之書籍以醫事法規為大宗,著重藥事法規者則較少見。因此,本文將介紹一本剛出版上市的新書《藥事法規實務應用》,該書為少數以藥事法規為主軸之專書。
我國西藥之專利連結制度,使學名藥廠之學名藥是否有侵害專利藥廠之原廠藥疑慮得以提早釐清,是非常重要的制度。此外,對於生技及醫藥領域之專利從業人員而言,西藥之專利連結制度的運作及其相關法規範,更是絕對須知悉的。本文除介紹《藥事法規實務應用》一書外,亦將有關西藥之專利連結的運作及其相關法律規範一併簡介。

圖片來源 : shutterstock、達志影像
《藥事法規實務應用》一書內容簡介
《藥事法規實務應用》(下稱《本書》)一書內容包含藥事法、藥師法、管制藥品管理條例、毒品危害防制條例、藥害救濟法及醫療器材管理法。分述如下:
● 藥事法
《本書》詳盡介紹有關藥物、藥商、藥局之管理及西藥之專利連結的規定,除使藥商及藥局經營管理者能更知悉所規範之法律外,更藉由深入簡出的內容,讓讀者能了解藥事法。
● 藥師法
《本書》詳盡介紹有關開業或執業藥師所應知悉之規範,有利已開業或執業之藥師或未來計畫開業或執業之藥師明瞭現行法律之各種規定。
● 管制藥品管理條例
《本書》詳盡介紹使用管制藥品、開立管制藥品專用處方箋、調劑管制藥品及簿冊登載等規定,以供相關人員留意,避免違反規定而受罰鍰處分。
● 毒品危害防制條例
《本書》詳盡介紹與毒品相關之各行為及其處罰,期望能藉由《本書》之介紹,減少毒品危害,以維護社會秩序。
● 藥害救濟法
《本書》詳盡介紹與藥害救濟相關之規定,使已生藥害者或未來若有申請需求者,能更了解藥害救濟之流程及預先判斷是否能順利獲得救濟。
● 醫療器材管理法
《本書》詳盡介紹與醫療器材相關之法規範,使醫療器材商及讀者能更深入了解此較新之法規。
《本書》除了各相關法規介紹外,更於各相關法規中適時提供實務案例,以便讀者能更知悉該法規之操作及實務所生之疑義。《本書》各法規末皆附有與藥師高考、藥事相關之公務員高考三級、關務三等,以及薦任升等考之歷屆試題,能讓各該考科之備考者於申論題答題能更言之有理外,選擇題答題亦能駕輕就熟。
西藥之專利連結制度與相關法規範
2017年12月29日立法院三讀通過藥事法部分條文之修正草案,建立了台灣的專利連結制度,2018年1月31日業經總統令公告,並於2019年7月1日公布西藥專利連結施行辦法。
與西藥之專利連結制度相關之法規範有藥事法的第四章之一西藥之專利連結 (條文部分為藥事法第48 - 3條至第48 - 22條),以及專利法的第60 - 1條。
西藥之專利連結制度之相關運作
● 登錄專利資訊
圖1為西藥之專利連結制度之相關運作簡圖。於我國,當專利藥廠領取新藥藥品許可證後,即為藥事法中之新藥許可證之所有人。藥事法第48 - 3條第1項規定,新藥藥品許可證所有人認有提報藥品專利權專利資訊之必要者,應自藥品許可證領取之次日起45日內,檢附相關文件及資料,向中央衛生主管機關為之;逾期提報者,不適用本章規定。因此,若專利藥廠認有提報藥品專利權專利資訊之必要,須於領取新藥藥品許可證之次日起45日內登錄專利資訊。前述專利資訊之內容則規定於藥事法第48 - 4條。
圖1. 西藥之專利連結制度之相關運作簡圖
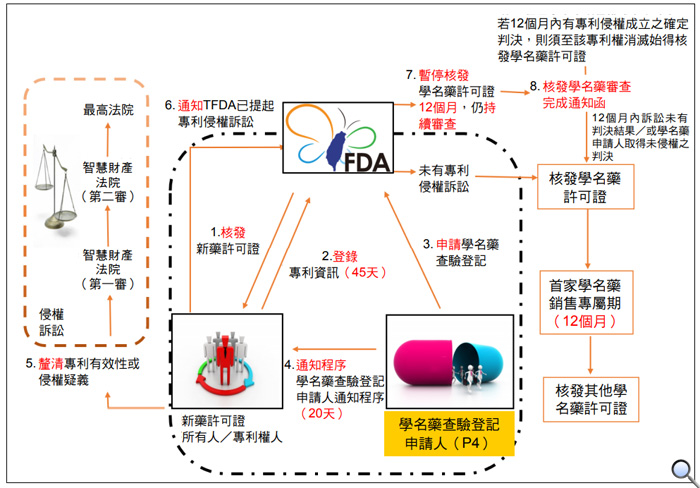
圖片來源:淺談台灣西藥專利連結制度[1]文章
● P4聲明及通知專利權人
當學名藥廠向我國食藥署申請學名藥藥品許可證時,即為藥事法中之學名藥藥品許可證申請人。藥事法第48 - 9條第1項規定,學名藥藥品許可證申請人,應於申請藥品許可證時,就新藥藥品許可證所有人已核准新藥所登載之專利權,向中央衛生主管機關為各款(該新藥未有任何專利資訊之登載(P1)、該新藥對應之專利權已消滅(P2)、該新藥對應之專利權消滅後,始由中央衛生主管機關核發藥品許可證(P3)或該新藥對應之專利權應撤銷,或申請藥品許可證之學名藥未侵害該新藥對應之專利權(P4))情事之一之聲明。於前述4款之聲明中,學名藥廠主要會聲明同條之第4款,即「該新藥對應之專利權應撤銷,或申請藥品許可證之學名藥未侵害該新藥對應之專利權」,簡稱P4聲明。食藥署審核學名藥廠所提出之文件後,認為文件齊備時,會核發學名藥廠藥品許可證申請資料齊備通知。
依藥事法第48 - 12條第1項規定,學名藥藥品許可證申請案涉及第48 - 9條第4款之聲明者,申請人應自中央衛生主管機關就藥品許可證申請資料齊備通知送達之次日起20日內,以書面通知新藥藥品許可證所有人及中央衛生主管機關;新藥藥品許可證所有人與所登載之專利權人、專屬被授權人不同者,應一併通知之。因此,學名藥廠須於藥品許可證申請資料齊備通知送達之次日起20日內,通知專利藥廠與專利權人,並依同法第48 - 12條第2項規定,就其所主張之專利權應撤銷或未侵害權利情事,敘明理由及附具證據。
● 侵權訴訟及銷售專屬期
依藥事法第48 - 13條第1項規定,專利權人或專屬被授權人接獲前條第1項通知後,擬就其已登載之專利權提起侵權訴訟者,應自接獲通知之次日起45日內提起之,並通知中央衛生主管機關。因此,專利權人若認為有侵權疑義時,須於接獲學名藥廠之通知次日起45日內提起侵權訴訟。依同條第2項之規定,此時,食藥署會暫停核發學名藥藥品許可證12個月。若於前述12個月內未有訴訟判決結果或學名藥廠取得未侵權之判決,食藥署會核發學名藥藥品許可證予學名藥廠。依藥事法第48 - 16條第1項規定,依第48 - 9條第4款聲明之學名藥藥品許可證申請案,其申請資料齊備日最早者,取得12個月之銷售專屬期間;中央衛生主管機關於前述期間屆滿前,不得核發其他學名藥之藥品許可證。因此,首家P4聲明之學名藥廠,依規定將可獲得12個月的銷售專屬期。
● 提起確認訴訟之規定
2022年4月15日專利法新增第60-1條之規定,第1項藥品許可證申請人就新藥藥品許可證所有人已核准新藥所登載之專利權,依藥事法第48 - 9條第4款規定為聲明者,專利權人於接獲通知後,得依(專利法)第96條第1項規定,請求除去或防止侵害。第2項專利權人未於藥事法第48 - 13條第1項所定期間內對前項申請人提起訴訟者,該申請人得就其申請藥品許可證之藥品是否侵害該專利權,提起確認之訴。因此,依專利法第60-1條第1項之規定,專利權人於接獲P4聲明之學名藥廠通知後,得依專利法第96條第1項規定,請求除去或防止侵害。惟若專利權人逾期未提起侵權訴訟時,依同條第2項之規定,P4聲明之學名藥廠得就其申請藥品許可證之藥品是否侵害該專利權,提起確認之訴,以此確認是否有侵害專利權。
備註:
- 吳秀梅,淺談台灣西藥專利連結制度,專利師,2019 年7 月,第39 期,頁2。
【本文僅反映專家作者意見,不代表本報立場。】
 |
|
| 作者: |
郭廷濠 |
| 現任: |
中華民國專利師 |
| 學歷: |
台科大專利所碩士 |
| 專長: |
1. 藥物藥理學
2. 生技、醫藥專利
3. 藥事、專利法規 |
| 證照: |
109年度中華民國專利師考試及格 |
|
|
|
| Facebook |
|
在北美智權報粉絲團上追踪我們 |
     |
|
|
|
|
|
|
|

